In einer Laboranalyse werden Proben auf unterschiedlichste Parameter untersucht. Manchmal will man den Anteil eines gewissen Stoffes wissen, beispielsweise bei den Inhaltsstoff-Angaben in der Lebensmittelkennzeichnung. Wieviel Zucker enthält das Produkt und wieviel Fett?
Und manchmal will man wissen, ob ein bestimmter Stoff überhaupt vorhanden ist. Für Allergiker stellt sich vielleicht die Frage, ob das jeweilige Lebensmittel Spuren von Nüssen oder Ei enthält. Wer seinen Garten in der Nähe eines Feldes hat, der kann und sollte daran interessiert sein, ob sich in seiner Gartenerde Spuren von Glyphosat oder anderen Pestiziden befinden.
Die Laboranalytik hat im Laufe der Jahre viele unterschiedliche Methoden, Verfahren und Messtechniken entwickelt, die schnelle und zuverlässige Ergebnisse liefern können.
Auf dieser Seite stellen wir Ihnen die wichtigsten Methoden vor. Viele dieser Messtechniken kommen bei unseren Analysen und in unseren Partner-Laboratorien zum Einsatz.
my-lab International bietet Laboranalysen für die verschiedensten Parameter in den unterschiedlichsten Materialien an, beispielsweise Weichmacher in Kinderspielzeug, Schwermetalle im Boden oder Pestizide in Lebensmitteln (–> zum Analysenshop für Privatkunden, für Geschäftskunden, für Laboratorien)
Allgemein: quantitative Analysen und qualitative Analysen

Laboranalysen unterscheidet man in qualitative und quantitative Analysen.
In der qualitativen Analyse wird ermittelt, woraus ein Stoff besteht. Angenommen, ein Stoff ist ein Glas voller Smileys, und die Smileys sind die Elemente bzw. Ionen (anorganische Stoffe) oder funktionelle Gruppen (organische Stoffe), dann ermittelt die qualitative Analyse, welche Art Smileys vorhanden sind.
In der quantitativen Analyse geht es nun darum, sich auf einen Bestandteil festzulegen, und herauszufinden, in welcher Menge er vorhanden ist. Um bei unserem Wasserglas zu bleiben: eine quantitative Analyse könnte die Fragestellung sein, wie oft der wütende Smiley im Glas vorkommt. Voraussetzung für diese Analyse ist natürlich, dass wir bereits über das Vorkommen der wütenden Smileys informiert sind. Eine quantitative Analyse setzt also die Erkenntnisse der qualitativen Analyse voraus.
 Chromatographie
Chromatographie
Das Prinzip der Chromatographie wird in der chemischen Analytik häufig in unterschiedlichen Formen verwendet. Unter Chromatographie versteht man das Auftrennen von einem Stoffgemisch in seine einzelnen Bestandteile. Dazu werden bei allen Verfahren immer zwei Phasen benötigt, eine stationäre und eine mobile Phase. Das Stoffgemisch wird mit der mobilen Phase über die stationäre Phase geleitet. Die einzelnen Komponenten aus dem Stoffgemisch gehen unterschiedlich starke Wechselwirkungen mit der stationären Phase ein. Das ist die Retention.
Die Komponenten werden unterschiedlich schnell transportiert. Das Gemisch trennt sich in einzelnen Bestandteile auf. Am Ende des Trennsystems ist ein Detektor installiert. Der Detektor misst, wann die einzelnen Bestandteile die stationäre Phase überwunden haben. Die benötigte Zeit zum Durchlaufen der stationären Phase ist die Retentionszeit.
Vorstellen kann man sich das ungefähr so wie bei einem Langstreckenlauf. Alle starten gleichzeitig, aber je nach Konstitution, Rückenwind und Beweglichkeit kommen die Sportler zu unterschiedlichen Zeiten im Ziel an.

Dabei steht dann jeder Läufer für eine Stoffgruppe im Stoffgemisch, die Strecke für die stationäre Phase und der Rückenwind für die mobile Phase. Der Detektor wäre dann die Ziellinie.
 Die Gaschromatographie
Die Gaschromatographie
In der Gaschromatographie (GC) besteht die mobile Phase aus einem Gas und die stationäre in der Regel aus einem Feststoff. Angewendet wird die Methode für Substanzen, die leicht verdampfen und in der Gasphase stabil sind.
Das Stoffgemisch wird in einem Injektor verdampft und dann mit einem Gas durch eine dünne Kapillare als stationäre Phase geleitet. Am Ende der Kapillare (Säule) misst ein Detektor alle Stoffgruppen, die das Trennsystem verlassen.
Die Gaschromatographie lässt sich mit verschiedenen Detektoren kombinieren:
- FID (Flammenionisationsdetektor)
- NPD (Stickstoff-Phosphor-Detektor)
- FPD (Flammenphotometrischer Detektor)
- MS (Massenspektrometer)
- MS/MS (Tandemmassenspektrometer)
 Die Flüssigkeitschromatographie (LC)
Die Flüssigkeitschromatographie (LC)
In der Hochleistungsflüssigkeitschromatographie, kurz HPLC (engl. high performance liquid chromatography) besteht die mobile Phase aus einer Flüssigkeit (Eluent oder Elutionsmittel). Diese Methode eignet sich gut für Substanzen, die nicht verdampft werden können. Das Stoffgemisch wird mittels einer Injektionsspritze und einem vorgeschalteten Ventil auf die Säule mit der stationären Phase aufgegeben und durch das Fließmittel (Eluent) über die Säule transportiert. Ein Detektor misst alle Stoffgruppen, die das Trennsystem verlassen.
Die Flüssigkeitschromatographie lässt sich mit verschiedenen Detektoren kombinieren:
- UV-Detektor
- Massenspektrometer (MS)
- Tandemmassenspektrometer (MS/MS)
- Fluoreszensdetektor
 Massenspektrometrie
Massenspektrometrie
Die Massenspektrometrie ist wohl das am meisten verwendete Verfahren, um organische und auch anorganische Substanzen zu bestimmen und zu analysieren. Die Massenspektrometrie wird dabei gekoppelt mit de Gaschromatographie (GC) und der Hochdruckflüssigchromatographie (HPLC).
Schematisch lässt sich die Massenspektrometrie in drei Schritten darstellen:
- Ionisation und Fragmentierung
- Trennung
- Detektion
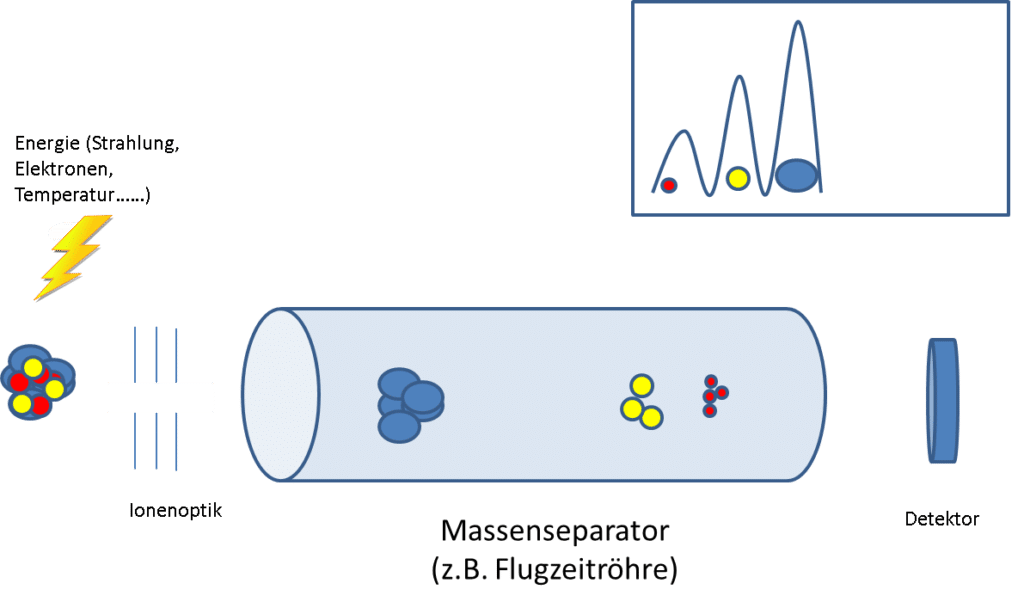
Bei der Ionisierung in der sogenannten Ionenquelle werden die einströmenden Moleküle durch Zufuhr von Energie zerlegt in Fragmente mit und ohne Ladung. Fragmente mit Ladung bezeichnet mal als Ionen. Die Zufuhr von Energie kann erfolgen durch Kollision mit Elektronen oder anderen Ionen, durch Strahlung (z.B. Licht) oder durch Temperaturerhöhung. Die unter den gegebenen Bedingungen entstehenden Ionen und Fragmente sind spezifisch für die zerlegte Substanz; d.h. die Substanz wird unter diesen Bedingungen immer in gleicher Weise zerfallen.
Bei der Trennung werden die geladenen Fragmente nach Masse bzw. nach dem Verhältnis Masse/Ladung getrennt. Auch hierfür kommen unterschiedliche Separatoren zum Einsatz: Quadrupol, Sektorfeldgeräte mit elektrischem und magetischem Feld, Ionenfallen, Flugzeitmassenspektrometer.
Der Detektor detekiert die separierten Ionen und liefert ein Signal, welches zur Menge an auf den Detektor prallenden Ionen proportional ist.
 ICP/MS
ICP/MS
Massenspektrometrie mit induktiv gekoppeltem Plasma. (englisch: inductive coupplet plasma). Unter Plasma versteht man ein elektrisch leitendes Gas. In diesem Fall wird Argon verwendet. Das Argon wird auf über 8000K aufgeheizt. Bei diesen Temperaturen liegt das Argon ionisiert vor und ist somit leitfähig. Man verwendet dieses Verfahren zur Analyse von anorganischen Elementen. Es wird für Schwermetalle und Spurenelemente eingesetzt.
Die Elemente werden in Lösung gebracht, zerstäubt und mit einem Argon Strom in das Plasma eingebracht. Die entstehenden Ionen werden im Massenspektrometer über ihr Masse/Ladungsverhältnis getrennt und am Detektor erfasst.
 Atomabsorptions Spektrometrie (AAS)
Atomabsorptions Spektrometrie (AAS)
Grundlage dieses Messprinzips ist die Wechselwirkung zwischen Licht und Atom. Die Elektronen eins Atoms besetzen im Grundzustand das möglichst niedrigste Energieniveau. Im Atom gibt es zahlreiche weitere Energieniveaus, die aber energetisch höher liegen. Bestrahlt man die Atome mit Licht einer bestimmten Wellenlänge, nehmen sie das Licht auf, und die Elektronen nehmen ein höheres Energieniveau ein.
Bei der AAS wird die Abschwächung des Lichts gemessen. Zum Vergleich werden Lösungen mit bekannter Konzentration eines Elements gemessen. Dann kann die Konzentration in der Probe berechnet werden.
 Röntgenfluoreszenz Analytik
Röntgenfluoreszenz Analytik
Bei der Röntgenfluoreszenzanalytik werden die Prinzipien der Röntgenstrahlung und der Fluoreszenzspektroskopie angewendet. Durch die Röntgenstrahlung werden Elektronen, die nahe am Atomkern sitzen, herausgeschlagen. Elektronen, die weiter Außen in der Atomhülle sitzen, nehmen deren Platz ein. Dabei wird Energie frei. Diese wird in Form von Fluoreszenzstrahlung abgegeben und kann gemessen werden. Diese Methode ermöglicht eine zerstörungsfreie Analytik. Das Objekt wird in die Messkammer gestellt, die Oberfläche wird bestrahlt, und der Gehalt kann bestimmt werden. Limitierender Faktor ist dabei die Größe der Messkammer. Prinzipiell können alle Elemente ab der Ordnungszahl 5 (Bor) analysiert werden. Gut geeignet ist dieses Verfahren für die Bestimmung von Metallen.
 Photometrie
Photometrie
Die Laboranalytik macht sich mit der Photometrie bestimmte Eigenschaften von Lichtwellen zunutze, um Konzentrationen zu bestimmen.
Um diese Analysenmethode zu verstehen, muss man sich zunächst bewusst machen, was Licht ist. Licht ist eine elektromagnetische Welle, die von der Lichtquelle ausgeht und schließlich von unserem Auge wahrgenommen wird.

Die Farbe des Lichts wird von der Frequenz der Welle bestimmt, wobei anzumerken ist, dass das menschliche Auge nur einen sehr geringen Teil der möglichen Lichtwellen Frequenzen wahrnehmen kann. Das bekannteste Beispiel aus dem Alltag dürfte hierzu das Infrarotlicht sein: fast jede Fernbedienung sendet ihre Signale per Infrarot zum Empfangsgerät, doch nicht einmal bei absoluter Dunkelheit können wir das Lichtsignal sehen. Halten wir jedoch eine Digitalkamera vor die Fernbedienung, dann sieht man im Display der Kamera das Lichtsignal der Fernbedienung. Der Grund: der digitale Sensor der Kamera ist sensibler als das menschliche Auge.
Es war Isaac Newton, der in einem abgedunkelten Raum weißes Licht auf ein Prisma lenkte und so feststellte, dass man das Licht in seine Spektralfarben aufbrechen kann. Anhand des Regenbogens, der aus dem Prisma heraus kam, konnte man die unterschiedlichen Frequenzen der Wellen mit den dazugehörigen Farben ableiten.
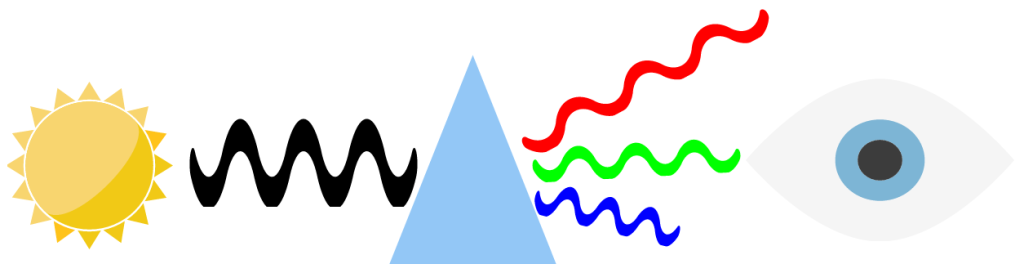
Genau diese Eigenschaft des Lichtes, die unterschiedlichen Farben bei unterschiedlichen Frequenzen, nutzt die Photometrie. Stark vereinfacht ausgedrückt wird ein Lichtstrahl durch eine Probe geschickt, die zuvor in eine spezielle Lösung gegeben wurde. Nun schaut man, welche Lichtstrahlen am anderen Ende der Lösung herauskommen und welche von der Lösung absorbiert wurden. Diese Lichtundurchlässigkeit nennt man „Extinktion“.
Mithilfe des Lambeert-Beersche Gesetzes lässt sich auf Basis des „Restlichtes“ errechnen, welche Spuren von welchen Substanzen in der Probe sind.
Weiterführende Links zur Photometrie
- http://www.filmscanner.info/Fotometrie.html – Hier geht es weniger um die Analytik, als vielmehr eine Einführung in die Grundbegriffe des Lichts. Es wird sehr schön erklärt was Begriffe wie Lumen, Candela und Steradiant bedeuten. Für den Einstieg in die Thematik unabdingbar.
- MKA Photometrieeinfuehrung – Eine weitere Einführungsseite, die sich mit der Photometrie als Analysenmethode beschäftigt. Auch wenn die Seite selbst technisch nicht auf dem neuesten Stand ist und die Darstellung auf Mobilgeräten am Rand abgeschnitten sein könnte, so gibt sie inhaltlich doch sehr schön wieder, was genau bei der Photometrie eigentlich passiert, und auch was es mit dem Lambeert Beersche Gesetz auf sich hat. Wer tiefer in die Materie einsteigen will, der ist hier genau richtig.
- http://www.git-labor.de/photometrie-kompendium – Hier kann man die Photometrie in einer kleinen Videoreihe in der Praxis sehen. Die Folgen lassen sich direkt und werbefrei anschauen (streamen). Sie bieten einen hohen Informationsgehalt und können durch angenehmen Schnitt ohne Effekthascherei überzeugen.
 Accelerated Solvent Extraction (ASE)
Accelerated Solvent Extraction (ASE)
ASE steht für Accelerated Solvent Extraction, was soviel bedeutet wie „Beschleunigte Lösemittelextraktion“. Das Verfahren ist außerdem unter dem Namen Pressurized Liquid Extraction (PLE) bekannt.
Bei einer Laboranalyse nach dem ASE Verfahren werden Inhaltsstoffe auf festen und halbfesten Proben gelöst. Dies wird erreicht, indem die Probe unter hoher Temperatur und hohem Druck gesetzt wird.
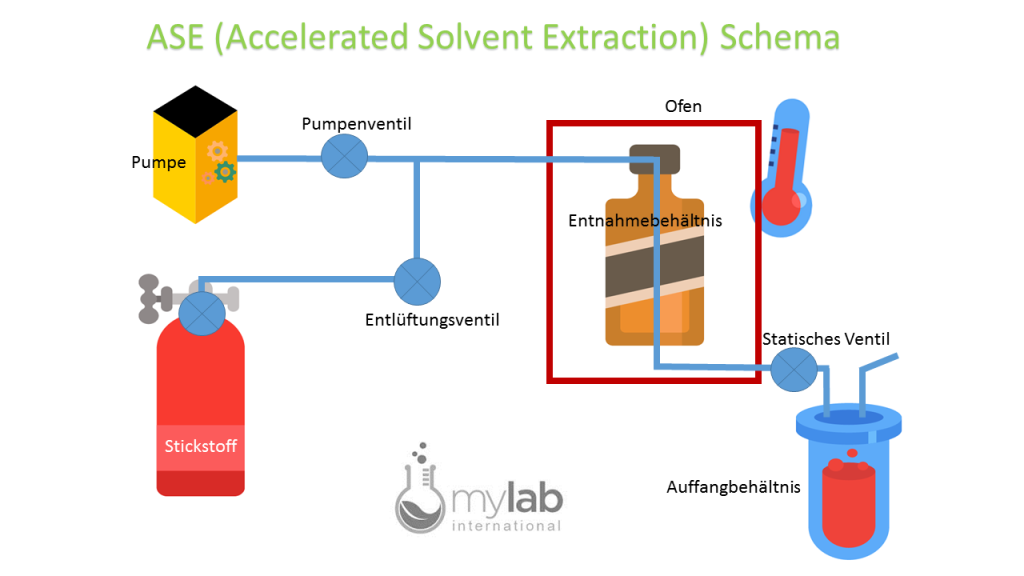
Das ASE Verfahren wurde 1995 in der Analytik eingeführt. Es entstand aus der Notwendigkeit heraus, dass das klassische Herauslösen von Inhaltsstoffen mit Lösemitteln zu zeit- und kostspielig wurde. Durch die erhöhte Temperatur lässt sich der zu untersuchende Inhaltsstoff wesentlich schneller extrahieren, ohne dass die Qualität der Analyse darunter leidet.



